在酶活性检测中,多采用物理的或化学的方法.在特定的最适条件下,测定酶催化反应中底物的消失量或产物的生成量,并用单位时间内的所述数量来表征酶的活性(终点法或总变量法);或者,根据Michaelis-Menten方程,求出供试酶类的Km和Vmax值(动力学法).下面就介绍酶活性测定的方法之一,电化学法。
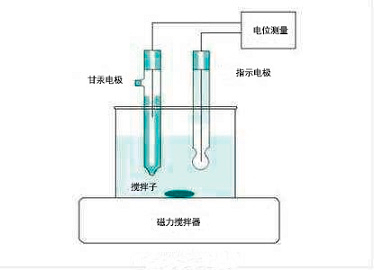
1.电位法
在酶催化反应进行的过程中,会产生电位的变化,这种变化与供试溶液中物质的浓度和性质有关,因此,可作为酶活性的量度.例如,胆碱酯酶在催化硫代胆碱酯的水解时,生成的硫醇的氧化今位比底物的要低,由此产生一电位降. 根据单位时间里的电位降,即可求出该种酶的活性。
许多酶催化反应的产物或底物中含有酸或碱,因此,可利用玻璃电极测定反应进行中的pH变化,以了解该反应的进程.由于pH的变化会影响酶的活性,从而影响反应进程, 因此一般不直接测定pH的变化,而代之以恒pH滴定法,即不断地加入碱(或酸)使pH保持恒定.为维持这一恒定所加入的碱(或酸)量,即为该反应的速度的量度.这种方法可用于研究酯的酶解。
需要指出的是,由于电极与溶液间的电子转移而引起的电位变化无法直接测出,因此,浸入供试浓液中的指示电极需与一电位固定的参比电极相连,组成原电池.通过测量原电池的电动势,来求得溶液中待测物质的浓度变化.
2.离子选择性电极法
该法是前些年迅速发展起来的测试方法,它是根据电极的膜电位对溶液中某一特定离子活度的响应来进行测定的.氨电极等气敏电极被用来测定生成NH3气等气体的酶反应进程.氨电极内部由一支平底的pH玻璃电极作为指示电极,浸泡在0.01摩尔/升NH4Cl和惰性电解质的内充液中,内充液与试液之间用一层极薄的透气聚偏氟乙烯膜隔开,参比电极为Ag-AgCl电极,也插在内充液中.测量时,试液产生的NH3气通过透气膜扩散、并溶于内充液时,pH玻璃电极指示内充液中〔OH〕的变化,直接反映〔NH3)的变化,从而了解产NH3催化反应的进程.
还有一些其他的离子选择性电极,如NH+4 、C02、I-、CN-等电极,也常用于研究酶催化反应.由于离子选择性电 极法设备简单,操作方便,并能进行伕速连续测定.因此,这类电极深受酶学工作者的关注.
3.电导法
若往供试溶液中浸入两个电极并在它们之间加一恒定电压,则在反应进行的过程中会产生电流的变化.后者取决于溶液的电导.它是溶液中所有离子的电导的总和,且为电极间电阻的倒数.对底物转化为产物时带电物质数会发生变化的酶催化反应说来,可以根据电导随时间的变化来了解反应的进程.这种方法称为电导法。在采用这种方法时,通常用交流电,而不用直流电,以防止电解的产生(它会降低所加电压)。由于反应混合物中需加入缓冲液、而它会产生一电导背景值,所以通常多采用低浓度的低内电导缓冲液(例如三羟甲基氨基甲烷缓冲液)。
脲酶催化的反应是适于用电导法进行酶活性测定的一个例子:反应进行时,不带电的尿素分子转化为氨离子,从而电导必然增大.在底物浓度小于22μmol•L-1时,,转化率与电导成直线相关.
4.极谱法
往浸入供试溶液的两电极间加一逐渐增大的电压,会引起扩散电流的变化.而溶液的组成,决定了某一瞬间流过的电流量,据此进行酶活性测定的方法称为极谱法.
曾根据胆碱酯酶催化碘化乙酰硫代胆碱也成硫醇时的电 流变化值来测定该种酶的活性.也曾用所述方法测定过氧化氢酶和3-羟基邻氨基苯甲酸氧化酶的活性.
此外,极谱氧电极也被普遍用于耗氧性酶催化反应体系的测定.这种电极由一金或铂中央阴极和一银环形阳极所组成,其间隔以环氧树脂套.该电极通过薄膜与供试液接触.溶解在反应混合物中的氧可通过薄膜自由地扩散到电压稳定在0.8V的阴极上,产生电化还原,从而使阳极和阴极间形成电流.该电流量正比于试液的p02,测定该电流量随时间的变化.便可获知酶催化反应过程中氧的生成或消耗的情况.它比起测压法来要敏感得多.
总的说来,与某些其他方法(如分光光度法测定酶活性)比较,电化学法突出的优点是,存在在悬液里的杂质通常不影响测定结果
独立公正 方法科学 规范严谨 服务周到

