1.原理
硝酸还原酶是植物氮素同化的关键酶,也是一种诱导酶,与作物吸收和利用氮肥有关,可催化硝酸盐还原为亚硝酸盐:
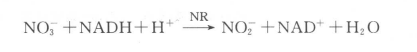
产生的NO2-在酸性条件下可以与对氨基苯磺酸(sulfanilic acid)或磺胺(对氨基苯磺酰胺,sulfanil-amide)反应生成重氮盐,再与α-萘胺反应生成红色偶氮化合物(对苯磺酸偶氮-α-萘胺)。
生成的红色偶氮化合物在520 nm波长下有最大吸收值,可用分光光度法测定。硝酸还原酶活性可以每小时每克鲜重产生的NO2- μg 数表示酶活性(NO2- μg·g-1FW·h-1)。
根据材料处理不同可分为活体法与离体法,根据反应介质的不同则可分为内源基质法和外源基质法。活体法步骤简单,适合快速、多组测定。离体法复杂,但重复性较好。内源基质法测定结果可反映硝酸还原酶在实际生长条件下的还原力,而外源基质法测定结果则可反映硝酸还原酶的潜在或最高还原力。下面介绍活体法的具体实验步骤。
2.试剂
(1).0.1 mol·L-1 pH7.5磷酸缓冲液:Na2HPO4·12H2O取30.0905g与Na2HPO4·2H2O取2.4965g,用蒸馏水定容至1000 mL。
(2).30%的三氯乙酸:30g三氯乙酸,蒸馏水溶后定容至100mL。
(3).0.2 mol·L-1 KNO3:20.22g KNO3用蒸馏水定容至1000 mL。
(4).磺胺试剂:1g 磺胺,加25mL 浓盐酸,用蒸馏水定容至100mL。
(5).α-萘胺试剂:0.2g α-萘胺,用含1 mL浓盐酸的蒸馏水定容至100mL。
(6).5 μg·mL-1 NO2-1标准液:0.10g NaNO2用蒸馏水定容至100mL,吸取7.5mL,再用蒸馏水定容至1000mL。
3.材料
欲测植物材料(如叶菜类蔬菜,实验材料在实验前一天可用硝态氮肥处理,以增强硝酸还原酶活性)。
3.方法步骤
(1)标准曲线制作:取7支15mL 刻度试管,按下表顺序添加试剂。
| 试管编号 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 5 μg·mL-1 NO2-1标准液/mL | 0 | 0.2 | 0.4 | 0.8 | 1.2 | 1.6 | 2.0 |
| 蒸馏水/mL | 2.0 | 1.8 | 1.6 | 1.2 | 0.8 | 0.4 | 0.0 |
| 每个试管中NO2-1含量/(μg·mL-1) | 0 | 0.5 | 1.0 | 2.0 | 3.0 | 4.0 | 5.0 |
| 磺胺及α-萘胺 | 每管加磺胺试剂2mL,α-萘胺试剂2mL,然后静置30min | ||||||
| 520 nm比色,吸光度(A) | |||||||
| 回归曲线 | |||||||
| 实验结果 | ||||
| 空白 | 重复1 | 重复2 | 重复3 | |
| 鲜重 | ||||
| 吸光度(A) | ||||
| NO2-含量C/(μg·mL-1) | ||||
| 酶活性/(μg NO2-·g-1 FW·h-1) | ||||
| 平均值 | ||||
4.结果计算
从标准曲线中检出NO2-含量(μg·mL-1),以每小时每克鲜重产生的NO2-·μg数表示酶活性,计算方法:
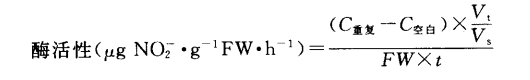
式中,C:根据回归曲线计算的NO2- μg数;Vt:反应液总体积(mL);Vs:测定时取样体积(mL);FW:鲜重(g);t:反应时间(h)。计算时,先分别计算3个重复的结果,再算平均值,为所求结果。
独立公正 方法科学 规范严谨 服务周到

