目的要求
利用氢氧化钠溶液滴定法测定果蔬中可滴定酸含量,了解可滴定酸含量对果蔬品质的影响。

基本原理
果蔬中含有多种有机酸,主要有苹果酸、柠檬酸、酒石酸、草酸等。果蔬种类、品种不同,所含有机酸的种类和数量也不同。果蔬中有机酸的种类和含量对果蔬的口味、风味、糖酸比、pH、贮藏性、加工性质都具有重要的影响。
果蔬可滴定酸(titritableacidity,TA)含量的测定是根据酸碱中和原理进行的,即用已知浓度的氢氧化钠溶液滴定果蔬提取液,根据氢氧化钠的消耗量计算果蔬中可滴定酸的含量。然而,由于每种果蔬中所含有的有机酸种类较多,在计算时,就要根据该果蔬中所含的主要种类有机酸进行折算。
材料、仪器及试剂
(一)材料
苹果、芒果、番茄等。
(二)仪器及用具
碱式滴定管( 20mL)、容量瓶( 100mL.1 000mL)、移液器,三角瓶( 100mL)、研钵、电子天平、漏斗、滤纸铁架台、蒸馏水。
(三)试剂
1、0. 1mol/L氢氧化钠溶液
称取4.0g分析纯氢氧化钠,加新煮沸过的蒸馏水溶解,待冷却后,再用新煮沸过的蒸馏水定容至1000mL,保存到带塑料盖的玻璃瓶中。
使用时,需用邻苯二甲酸氢钾溶液标定氢氧化钠滴定液。准确称取0.6000g在105℃干燥至恒重的基准邻苯二甲酸氢钾,加入50mL新煮沸过的冷水,振摇,使其尽量溶解。再滴加2滴1%酚酞指示剂,用配置的氢氧化钠溶液滴定。在接近终点时,应使邻苯二甲酸氢钾完全溶解,滴定至溶液呈粉红色。每1mL的NaOH滴定液(0.1mol/L)相当于20.42mg的邻苯二甲酸氢钾。根据NaOH溶液的消耗量与邻苯二甲酸氢钾的用量,计算出NaOH滴定液的浓度。
2、1% 酚酞指示剂
称取1.0g酚酞,加入到100mL50%的乙醇溶液中溶解。
(一)提取
称取混合均匀的果蔬样品10.0g(或吸取10.0mL汁液),置于研钵中磨碎,转移到100mL容量瓶中,再用蒸馏水冲洗研钵,-并转人到容量瓶中,并定容至刻度,摇匀。静置30min后过滤。
(二)测定
吸取20.0mL滤液,转人三角瓶中,加入2滴1%酚酞指示剂,用已标定的氢氧化钠溶液进行滴定。滴定至溶液初显粉色并在0.5min内不褪色时为终点(pH=8.1~8.3),记录氢氧化钠滴定液的用量,重复三次。再以蒸馏水代替滤液进行滴定,作为空白对照。
实验结果与计算
1.测定数据记录
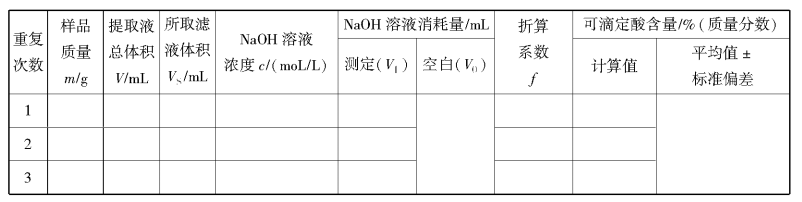
2.计算结果
根据NaOH滴定液消耗量,计算果蔬组织中可滴定酸含量,以质量分数(%)表示。计算公式:
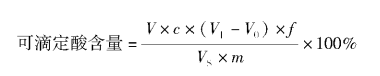
式中 V——样品提取液总体积,mL;
Vs——滴定时所取滤液体积,mL;
c——NaOH滴定液浓度,mol/L;
VI——滴定滤液消耗的NaOH溶液体积,mL;
Vo——滴定蒸馏水消耗的NaOH溶液体积,mL;
m——样品质量,g;
f一折算 系数,g/mmol。
折算系数,即在反应过程中中和1mmol氢氧化钠所需的有机酸的质量。果蔬中含有的有机酸种类较多,在计算可滴定酸含量时只需按照其中主要的有机酸进行折算即可。果蔬组织中常见的有机酸及其折算系数如下:
苹果酸——0.067(苹果、梨、桃、杏、李子、番茄、莴苣);
柠檬酸——0.064(柑橘类);
酒石酸——0.075(葡萄)。
注意事项
(1)一些果蔬中含酸量较少,利用0. 1mol/L NaOH溶液进行滴定时,NaOH溶液消耗的体积过小,容易引起较大的误差。在实际操作过程中,可以将NaOH滴定液适当稀释后使用。如利用0.05mol/L甚至0.01mol/L的NaOH溶液进行滴定。
(2)可滴定酸含量计算公式中的Vo为三次空白测定的平均值。
独立公正 方法科学 规范严谨 服务周到

